미래유망직업
[전문가칼럼] PTM 및 유전자 기술에 대하여
#여성과학기술인#유전자#DNA#PTM
조회수 2000
좋아요4
작성일2023-06-21
[전문가칼럼] PTM 및 유전자 기술에 대하여

카이스트 의과학대학원 이지민 교수
학력 : 서울대학교 생명과학부 이학사, 서울대학교 생명과학부 이학박사
경력 : 카이스트 의과학대학원 교수 (2022.02 - 현재)
강원대학교 분자생명과학과 교수 (2018.03 - 2022.02)
삼성바이오에피스 Business Development team 책임연구원 (2016.01 - 2018.03)
삼성전자 종합기술원 치료용항체그룹 Research Staff (2011.09 - 2015.12)
서울대학교 크로마틴 다이나믹스 연구단 Post.Doc (2010.09 - 2011.08)
1) 현재 연구 중이신 PTM 코드에 대해서 소개 부탁드립니다.
히스톤 단백질의 PTM 코드 - DNA 자체의 유전학만으로는 설명할 수 없는 비밀을 풀다.
우리 몸에서 실제 기능을 하고 있는 단백질은 센트럴 도그마(Central dogma)라는 과정을 거쳐서 생산되어진다. 즉 DNA 유전 코드에서 mRNA로 바뀌는 전사를 거치고 다시 mRNA가 단백질이 되는 번역과정을 통하여 구조적인 기능성을 가지게 된다. 단백질로 번역이 된다고 끝이 아니라, 이 이후의 과정이 단백질의 성능에 큰 영향을 끼친다는 사실이 알려지게 되었는데 이를 '단백질 번역 후 조절'(Post-Translational Modification·PTM)라고 한다. 예를 들어 종양 억제자라고 알려져 있는 p53 단백질도 특정 아미노산 잔기에 PTM 중 하나인 메틸화나 인산화가 유도되면 정반대 성격을 띄는 발암유전자(Oncogene)으로 바뀌게 되어, PTM 코드는 단백질이 번역이 되었다고 끝이 아니라 그 이후에 단백질의 성질을 완벽하게 탈바꿈 시킬 정도의 능력을 지니었다고 말할 수 있다. 이러한 PTM 코드는 단백질을 이루는 아미노산 20개 중 각 아미노산의 특성에 따라 다르게 일어나며, 하나 이상의 조합으로 발생되어 단백질의 기능적 다양성이 증폭되는 것으로 알려져 있어 이를 파악하는 것이 질병의 원리를 연구하는데 무엇보다 중요하다고 할 수 있다.
PTM코드의 영향을 받는 대표적인 단백질의 예로 히스톤을 들 수 있는데, 히스톤은 후성유전학이라고 하는 분야에서 핵심적인 역할을 수행하는 단백질이다. 히스톤이라는 구슬에 DNA라고 하는 실타래가 아주 규칙적으로 빽빽하게 감겨져 있기에 우리 몸을 이루는 아주 작은 세포 안 더 작은 핵 안에 유전 정보가 얽히지 않고 저장되어질 수 있는 것이다. 그러나, 히스톤 단백질에 DNA가 감겨져만 있다면 아무런 기능을 할 수 없고, 필요할 때에만 풀려나야하는데 이렇게 히스톤에서 DNA가 풀리고 감기고 하는 현상을 우리는 후성유전학의 하나라고 생각하며, 이는 유전 정보가 동일한 일란성 쌍둥이가 왜 다른 모습을 하게 되는지에 대한 근원적 대답으로 여겨지고 있다. 또 예를 들어 모든 벌들은 애벌레일 때 동일한 DNA를 가지고 태어나는데 로열젤리를 먹은 애벌레만이 여왕벌이 되고 나머지는 일벌이 되게 된다. 이러한 현상도 DNA 자체의 유전학만으로는 설명할 수 없고 히스톤 단백질에 풀렸다 감기는 DNA의 후성유전학으로만 설명이 가능하다. 그렇다면 언제 히스톤에서 DNA가 풀리고 또 언제 감기게 되는 것일까? 이것을 설명해줄 수 있는 것이 바로 히스톤 단백질의 PTM 코드이다. 히스톤 단백질의 아미노산 서열 하나하나에 어떠한 PTM이 가능한 지 지도가 그려질 만큼(Histone map) 밝혀진 것도 많지만 지금 이 순간에도 지구 곳곳의 과학자들에 의해 새로운 히스톤의 PTM 코드 혹은 기존의 보고된 히스톤 PTM 코드 간의 새로운 크로스토크(crosstalk)가 연구되어지고 있으며 이는 미지의 생명 현상, 질병의 발병 원인, 치료 전략을 제시하는데 큰 역할을 하고 있다.
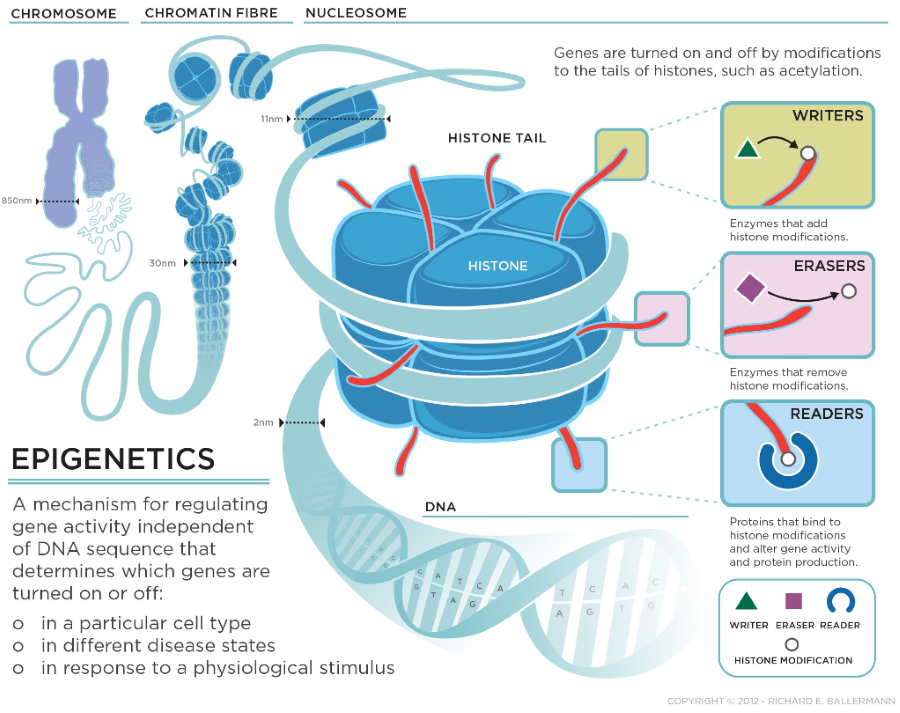 후성유전학(Epigenetics)에서 히스톤 단백질의 PTM 코드 ⓒ Zenith Epigenetics
후성유전학(Epigenetics)에서 히스톤 단백질의 PTM 코드 ⓒ Zenith Epigenetics
2) PTM코드 규명을 통해서 어떤 혁신을 기대할 수 있을까요?
PTM 코드 규명을 통한 혁신
위에서 언급한 PTM은 우리 몸 안에 존재하는 모든 단백질에 변형을 가할 준비가 되어 있으며 이 변형은 가역적이라고 할 수 있다. 즉, 변화를 유도하는(쓰는) 효소인 writer, PTM 변화를 제거하는(지우는) eraser, 더 나아가 두 개 이상의 PTM 변화를 연결할 수 있는(읽어서 다음 변화로 넘기는) reader 효소가 존재한다. PTM의 복잡하고 정교한 다이나믹스는 세포 내에서 혹은 세포 주변 환경에서 변화에 적응, 질병으로 가지 않고 부단히 정상 세포의 항상성을 지키기 위해 시시각각 일어나고 있다. 이러한 writer/eraser/reader 효소가 관여하는 PTM 코드는 후성유전학의 핵심 인자인 히스톤에 관여할 뿐 아니라 히스톤이 아닌 (혹은 포함한) 모든 단백질에 영향을 끼칠 수 있으며, 구체적으로는 표적단백질의 분해를 좌지우지할 수 있는 코드라고 할 수 있다. 센트럴 도그마인 DNA → mRNA → 단백질 에서 최종 산물인 단백질의 양을 조절하는 것은 기능적/구조적 실제 기능을 하는 단백질을 오래 작용 하게 할 수도 있으며, 잠깐 작용만 하고 사라지게 (분해되게) 할 수도 있는 것이다.
PTM 코드에 의하여
증가하는 단백질의 다양성과 복잡성 ⓒ Thermo Fisher
표적단백질 분해(Targeted Protein Degradation, TPD)는 질병을 유발하는 인자가 단백질로까지 번역(Translation)된 이후에 해당 단백질을 직접적으로 분해하여 없애는 기작을 의미하기에, 20년 전부터 이 기작을 실제 치료제로 개발하는 기술이 등장하였는데, 이는 표적단백질 분해제(Proteolysis-targeting chimera, PROTAC)로으로 대표되기도 한다. 실제 치료 기술에서도 PTM 코드를 이해하려고 노력하고 있기에 PTM 코드를 규명하는 것은 임상적으로도 매우 중요하다고 할 수 있다. 또한, 이는 기존에 세포 내에 존재하여 공격하기 어려웠던 질병 유발 단백질을 없앨 수 있는 치료제가 환자에게 적용되었다는 것을 의미하여, 기존 약물로 치료할 수 없는(Undruggable) TPD 대상 단백질을 약물의 치료가 가능한(Druggable) 대상으로 확장했다는 점에서 중요하다. 쉽게 이야기하자면 특정 아미노산에 PTM이 일어나야만 사라지는 단백질이 있다고 하자. 그런데 하필 그 단백질이 질병을 유발하는데 필수적인 역할을 한다면? PTM코드의 이해 없이는 질병 단백질을 절대 없앨 수 없는 것이다. 따라서 PTM 코드를 이해하는 것은 혁신적인 치료제 개발에 필수적이다.
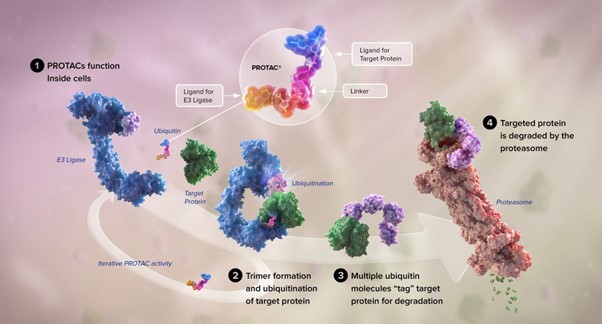
표적 단백질을 분해하는 기술인 PROTAC ⓒ ARVINAS
3) 현재의 유전자 과학의 수준은 어느 정도이며, 앞으로 어떤 부분에 대한 연구가 더 필요할까요?
현재 유전자 과학의 수준 및 향후 필요한 연구 분야
후성유전학(Epigenetics)는 유전자 자체만이 아니라 유전자 너머 (epi) 무엇이 더 있을 것이라는 전제의 학문이다. 질병에 걸리고 나면 되돌리는 건 어렵지만 질병으로 가기 전에 멈출 수 있다면, 그리고 혹여 어쩔 수 없이 질병으로 가는 세포라면 그 세포만 구분해 치료제를 투여할 수 있을텐데 그 기반이 되는 것이 후성유전학적 변형이라 할 수 있다. 히스톤의 PTM 코드가 후성유전학의 대표격으로 알려져 있지만, 히스톤을 포함한 생체 내 존재하는 모든 단백질이 PTM 코드의 영향을 받을 수 있어 개인적인 견해로는 비히스톤 단백질로의 PTM 코드 확장 연구가 정상세포가 내재적으로 언제 질병세포로 변하는지 이해하는데 향후 필요한 연구 분야라는 생각이 든다. 우리 몸 속에서는 세포가 현명한 전략으로 시시각각의 질병으로 변하는 자극을 원점으로 되돌리려 노력하지만, 자극이 중첩되어 어떠한 문턱값(threshold)을 넘을 때 질병으로 가게 되는데 이 내재적 변화의 스위치를 후성유전학, 그리고 PTM 코드의 이해를 통해 파악할 수 있으리라 믿는다.
4) 현재 연구팀의 전공 배경을 소개해주실 수 있으신가요?
후성유전 의공학 연구실 배경
후성유전 의공학 실험실에서는 핵 안에서 일어나는 후성유전학적 변화를 최대한의 생물학(Nature biology)을 이용하여 자연모사(Nature-inspired)한 후성유전자적 리프로그래밍(Epigenetic reprogramming) 활용 치료제를 발굴하는 것을 목표로 한다. 신규 후성유전학적 신호를 동시에 읽고 전달하는 크로마틴 에피 글루(Chromatin epi-glue)를 합성생물학(Synthetic biology)로 제작하는 것을 대표로 후성유전의공학(Epigenetic engineering) 기반 바이오소재를 치료제로 개발하고자 한다. 또한 암과 염증질환을 포함한 다양한 질병의 진행과 억제를 조절하는 세포 내 단백질들의 번역 후 조절 과정 (Post translational modification, PTM) 간의 상호작용(crosstalk) 다이나믹스를 밝히고자 한다. 새로운 단백질 데그론(degron) 코드를 이용한 암 대사(Cancer Metabolism)조절 단백질 정보 네트워크를 규명하는 목표를 가지고 있으며, 궁극적으로는 다양한 크로마틴 코드를 활용한 질병 제어 기술 및 기존 치료제에 저항성이 생기는 메커니즘에 기반한 심도 깊은 응용 연구도 진행하고자 한다. 실험실에서 필요한 기능과 기술로는 합성생물학, 후성유전학, 의약품개발(바이오소재), 의공학이며 치료 분야쪽으로는 암 대사(Cancer metabolism), 재생의학 그리고 중개 연구(Translation research)이다.
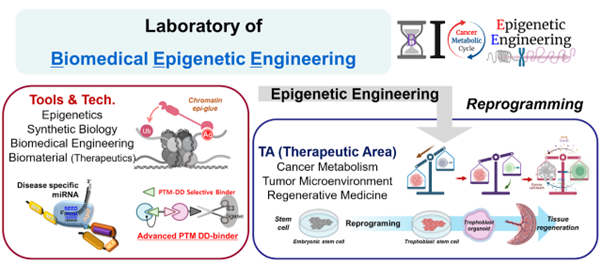
이지민 교수 연구실 연구 모식도 ⓒ Ji
Min's Lab - BEE Lab @KAIST GSMSE
5) 유전자 분야로의 진출을 꿈꾸는 학생, 예비 연구자분들이 꼭 갖추어야 하는 역량이 있다면 무엇일까요?
요즘의 연구에서는 대량의 정보를 분석해내는 것을 빼놓을 수 없다. 엄청난 분량의 염기서열분석(sequencing) 데이터를 분석해내고 이를 실험적으로 증명하는 것이 동시에 필요하다. 흔히 전통방식의 실험(wet work)과 정보매체 내에서만 진행하는 실험(dry work)으로 구분하여 선택하려고 하는데, 한 쪽에 더 집중하더라도 개방적인 마음으로 다른 영역의 실험기법, 분석법을 받아들일 수 있는 자세가 중요하다. 세포가 주변 환경과 서로 신호를 주고받으며 변화에 유전학/후성유전학을 총 동원하여 적응해 나가듯이 세포의 현명한 적응 기작을 이해하려는 과학자들도 개개의 영역들에 대한 이해를 바탕으로 소통하고 융합하여 과학적 현상을 규명해나가야 하므로 이러한 자세를 미리 배워나갔으면 좋겠다.
6) 앞으로 유전자 시장에 대한 전망 등에 대하여 자유롭게 말씀해주세요.
박사 학위 과정 중에 종양 억제자(Tumor suppressor)의 표적단백질 분해에 단백질 번역 후 변형(Post-translational Modification, PTM) 중 하나인 메틸화(Methylation)가 반드시 선행되어야 함을 메틸데그론(Methyl Degron)으로 연구하여 보고하였다. 회사 연구개발 부서에서 근무 시, 개발하여 임상 1상에 진입한 치료용항체 SAIT301의 효능 메커니즘을 연구할 때에 SAIT301이 타겟하는 c-Met이라고 하는 발암유전자(Oncogene) 단백질을 분해하는데 인산화(Phosphorylation)가 필수 선행 조건임을 발견하였다. PROTAC(Proteolysis-targeting chimera) 기술을 직접 이용하지 않아도 표적단백질 분해를 이해하는 것은 질병을 치료하는 신약개발에 있어 임상 적용 환자군을 선별하고 치료 기작을 설명하는데 중요하다는 것을 알게 되었다. 임상에서의 가능성이 검증되고 있는 표적단백질 분해 기술은 회사와 학교 모두에서 활발히 연구되고 있어 향후 다양한 질병 영역에서 활용될 것으로 기대되며, 환자에게 새로운 치료 기전을 제시할 것으로 기대된다.